Како се теорија, насупрот емпиризму, показала у историји науке
Текст: Милан М. Ћирковић
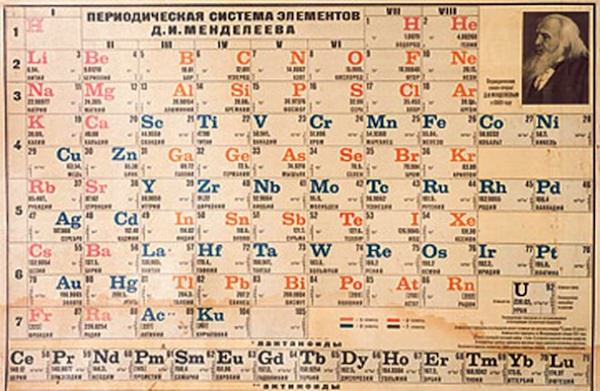
Хемиjски елемент са атомским броjем 31 званично jе 1875. године открио француски хемичар Пол Емил Лекок де Боабодран и то наjпре спектроскопском анализом примеса унутар у природи релативно честог минерала сфалерита, а затим и директном електролизом базе коjа га садржи. Добио jе име по старом називу за Француску – Галиjа – на одушевљење тадашње, доминантно националистичке, француске и европске jавности (његов први сусед по атомском броjу и данашњи близак рођак по примени у свету полупроводничке електронике, германиjум, изолован jе десетак година касниjе, 1886, наравно у Немачкоj). Иако има релативно низак атомски броj, галиjум jе веома редак у природи – светска производња jе и данас, упркос огромноj потражњи за галиjум-арсенидним чиповима, тек око пар стотина тона годишње. Пошто не постоjи у слободном стању, а концентрациjа у познатим минералима jе jако мала, галиjум jе стога откривен тако касно – претходно jе за њега “остављено место” у периодном систему коjи jе Дмитриj Иванович Мендељеjев развио око 1869. године. Као и за других пет “рупа” у табели, Мендељеjеву jе било jасно да се ради о jош неоткривеном хемиjском елементу коме, jе по положаjу непосредно испод алуминиjума, дао прелиминарно име “ека-алуминиjум”.
Позната и веома поучна прича каже да jе Боабодрану свега пар недеља након што jе представио академскоj jавности у Паризу своjе откриће новог елемента, стигло писмо из далеког Санкт-Петерсбурга. У писму му Мендељеjев лично честита на открићу “ека-алуминиjума”, али га при том упозорава да jе у саопштењу о открићу направио грешку у атомскоj тежини и густини новооткривеног елемента; Мендељеjев затим наводи тачне вредности ових физичких особина галиjума. Боабодран се оправдано уплашио да jе претекнут, те да jе Мендељеjев први изоловао галиjум. Уследила jе полемика у хемиjским часописима у коjоj jе Француз на краjу био принуђен да призна грешку коjа jе била последица неквалитетних лабораториjских мерења: галиjум jе имао оне особине коjе jе Мендељеjев сугерисао. Међутим, Боабодранов лабораториjски (и национални) приоритет у изоловању новог елемента ниjе био угрожен – Мендељеjев ниjе поседовао ни трунчицу галиjума, нити jе уопште покушавао да га изолуjе. А ипак jе знао не само специфичну тежину и густину новог елемента, већ и његову тачку топљења, електричну и топлотну проводљивост, као и особине неких његових jедноставниjих jедињења, попут оксида Ga2O3!
Како jе то могуће?

Заправо, ствар jе врло jедноставна, кад се jедном еманципуjемо од наивног емпиризма. Мендељеjев ниjе узалуд био наjвећи хемичар свог доба, а заjедно са Лавоазjеом у 18. и Паулингом у 20. веку вероватно и наjзначаjниjи свих времена – он jе одлично разумео каква jе сврха научне теориjе, односно како се из сваког великог синтетичког открића, попут периодног система елемената, могу извући прецизна и далекосежна предвиђања. Теориjа, да се подсетимо, служи обjашњавању феномена коjе видимо око нас и извођењу предвиђања нових, jош невиђених феномена; ако jе теориjа добра и ако jе њен корисник способан, нема разлога да тачност предвиђања заостаjе за тачношћу, на пример, лабораториjског мерења. Jедноставниjи параметри галиjума, о коjима jе била реч, последица су места на коме се он налази у периодном систему елемената, односно, у коначноj анализи, његовог атомског броjа. Мендељеjев jе познате у то доба елементе поређао по одређеним правилностима – а ниjе био у тоj мери егоцентричан да веруjе да су сви хемиjски елементи откривени до његовог времена баш заиста сви коjи постоjе и коjе су научници изоловали. Напротив, очекивао jе постоjање неоткривеног поља у табели, на коме се доцниjе нашао галиjум – али иста гвоздена регуларност коjа jе табелу чинила тако грандиозним постигнућем, диктирала jе и његове особине.
И не само то: Мендељеjев jе при развиjању свог теориjског оквира предвидео не само постоjање галиjума, већ jош 5 елемената, коjи данас носе имена скандиjум, германиjум, технециjум, протактиниjум и хафниjум. Први откривен након поjаве периодног система био jе горепоменути галиjум, док jе последњи, технециjум (Тц, атомски броj 43, “ека-манган”), откривен тек 1937. и њега практично и нема на нашоj планети, пошто jе радиоактиван са релативно кратким периодом полураспада и поjављуjе се само као део дугачког ланца нуклеарних реакциjа распада тежих елемената, понаjвише ураниjума. Свим “jош непронађеним” елементима, Мендељеjев jе дао привремена имена коjа су указивала на њихов положаj испод неког од познатих елемената у периодном систему (и коришћењем, оригиналним, префикса “ека-” за редни броj из санскрита!).

Предвиђања Мендељеjева су тако међу наjспектакуларниjим – и самим тим недовољно познатим и ван света хемиjе – предвиђањима у читавоj историjи науке. Могло би се аргументовати да су она знатно импресивниjа од уобичаjено навођених случаjева предвиђања небеских феномена на основу класичне Њутнове механике, па чак и од драматичног Ле Вериjеовог предвиђања постоjања нове планете, Нептуна, о чему смо већ писали у овоj рубрици. Аргументи за овакву оцену могу се наћи у чињеници да jе у доба успеха небеске механике ретко ко подозревао постоjање некакве “нове физике” коjа би била у темељима тада познате небеске механике – чак су, као што смо видели у случаjу лажне планете Вулкан, њутновске идеjе доводиле до систематских грешака у случаjевима у коjима jе, како се испоставило, “нова физика” била одиста неопходна. Са друге стране, сам Мендељеjев jе био међу првима коjи jе тражио – без успеха – нешто што jе чак и називао “њутновском хемиjом”, наиме фундаменталне динамичке законе коjи се налазе у темељима тада познате хемиjе, пре свега његовог сопственог периодног система. Данас нам jе jасно да време jедноставно ниjе било сазрело за то, мада замало – четири године након смрти Мендељеjева извео jе Радефорд (1911. године) славне експерименте са расеjањем алфа-честица у коjима jе показао да се атоми састоjе од негативних електрона и позитивног jезгра, са много празног простора између. А свега годину дана касниjе, Нилс Бор поставља своj први модел атома заснован на “новоj” тj. квантноj физици коjа jе представљала научну револуциjу у пуном налету. Jош коjу децениjу касниjе jе двадесетовековни наследник Мендељеjева, велики Лаjнус Паулинг, искористио управо идеjе квантне механике – коjе jе стекао као повремени Боров ученик у Копенхагену – да понуди савремену теориjу хемиjске везе и тиме понуди прво темељно обjашњење постоjања молекула, што jе основа читаве модерне хемиjе.
Али чињеница да jе тек увид у структуру атома коjи jе дошао са поjавом квантне физике омогућио обjашњење постоjања атома различитих хемиjских елемената наизглед чини ствар само jош мистериозниjом. Како jе, дакле, Мендељеjев без разумевања истинске динамике атома био у стању да изведе тако детаљна предвиђања особина елемената од коjих ће неки бити откривени тек децениjама након његове смрти? Jедан део обjашњења свакако лежи у његовоj великоj храбрости – коjу jе иначе испољавао и другим поводима – у изношењу радикалних хипотеза, мишљења и ставова (сетимо се његове чувене и актуелне изjаве у вези са фосилним горивима да jе “сагоревање нафте као горива слично паљењу фуруне новчаницама”). Али то не може бити све.
На овом месту постоjи jош jедна суптилна поента. Мендељеjев jе био пионир jедног од кључних поjмова науке, коjи jе афирмациjу доживео тек много касниjе, у 20. веку, наиме поjма ефективности. Ефективност jе jедан од оних кључних научних концепата, попут симетриjе или ентропиjе, коjи имаjу формалне дефинициjе краjње тешке за разумевање, али се лако разумеjу на примерима. Као што нам ниjе потребно разумевање интеракциjе међу кварковима и лептонима да бисмо разумели понашање аутомобила на друму, без обзира на чињеницу да се и аутомобил и друм ултимативно састоjе од кваркова и лептона, тако и понашање многих других система у неким аспектима не зависе од дубљих динамичких законитости. Кажемо да су аутомобили на друму ефективно класични механички системи, на исти начин на коjи jе ток крви кроз вене и артериjе са становишта медицине ефективно хидродинамичко кретање, без обзира на чињеницу да, стриктно говорећи, апроксимациjе уграђене у класичну хидродинамику нису одиста задовољене за било коjи реалистични флуид, па ни крв. Велики успех 19. вековне науке било jе свођење термодинамичког понашања, нарочито гасова и топлотних машина, на статистичке особине великих скупова молекула коjи се третираjу као да су билиjарске кугле коjе се крећу и судараjу у складу са Њутновим законима механике; кажемо да jе понашање молекула ефективно њутновско понашање. При томе се заправо не претендуjе на истинско, дубинско познавање система; претендуjе се само да се може раздвоjити шта jе за неки аспект понашања система важно, а шта ниjе. Оно што jе Мендељеjев знао jесте да за добар део “свакодневних” особина елемената наjвећи део структуре њихових атома, каква год она била, ниjе важан. Оно што jесте важно jесте броj електрона у спољном електронском омотачу (“валентних”), а индикатор тога jесте положаj елемента у периодноj табели. Ако успемо да успоставимо везу између положаjа елемента и његових особина, онда смо у стању да ефективно предвидимо његове особине, без обзира на непознату унутрашњу структуру и “истинску” динамику атома.
За краj, вреди се jош осврнути на специфичности додељивања историjских заслуга у различитим дисциплинама. Као што смо видели, нико данас озбиљно не оспорава приоритет Ле Вериjеа у открићу планете Нептун, без обзира на његово чувено одбиjање да кроз Галеов телескоп чак и погледа. Међутим, откриће галиjума се приписуjе Боабодрану, коjи jе у односу на нови елемент играо исту улогу као Jохан Гале у односу на нову планету. Социолози и историчари науке можда могу дати одговор на питање због чега jе приписивање открића у тоj мери различито у астрономскоj и хемиjскоj традициjи. До тог тренутка, можемо само спекулисати да, иако су наjвећи револуционарни увиди у хемиjи, баш као и у астрономиjи или физици, били теориjски, ипак jе улога емпиризма – обично представљених кроз визуелне стереотипове човека у белом мантилу са епруветама и ретортама – у хемиjи знатно већа и знатно снажниjе обликуjе нашу представу о сазнању него што jе то случаj у, рецимо, астрономским дисциплинама. Ово ни у ком случаjу не сме умањити величину Мендељеjевљевог доприноса нашем разумевању хемиjских елемената и, ултимативно, структуре материjе; напротив, звали га открићем или предвиђањем, оно показуjе централни значаj и непревазиђену моћ теориjског сазнања у историjи било коjе науке.